Giải bài 17 hóa học 12: Vị trí của kim loại trong bảng tuần hoàn và cấu tạo của kim loại
Theo dõi 1.edu.vn trênA - KIẾN THỨC TRỌNG TÂM
I. Vị trí của kim loại trong bảng tuần hoàn và cấu tạo của kim loại
Trong bảng tuần hoàn có gần 90 nguyên tố kim loại. Các nguyên tố kim loại có mặt ở:
- IA (trừ hiđrô); nhóm IIA, nhóm IIIA (trừ Bo) và một phần nhóm IVA, VÀ, VIA;
- Các nhóm B (từ IB đến VIIIB);
- Họ lantan và actini được xếp riêng thành 2 hàng ở cuối bảng.
II.Cấu tạo của kim loại
1.Cấu tạo nguyên tử
- Nguyên tử của hầu hết các nguyên tố kim loại đều có it electron ở lớp ngoài cùng (1,2 hoặc 3e).
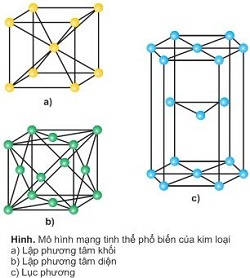
2.Cấu tạo mạng tinh thể
- Ở nhiệt độ thường, trừ thủy ngân ở thể lỏng, còn các kim loại khác ở thể rắn và có cấu tạo tinh thể
- Trong tinh thể kim loại, nguyên tử và ion kim loại nằm ở những nut mạng tinh thể. Các eletron hóa trị liên kết yếu với hạt nhân nên dễ tách khỏi nguyên tử và chuyển động tự do trong mạng tinh thể.
- Mạng tinh thể lục phương có độ đặc khít 74%.
- Mạng tinh thể lập phương tâm diện có độ đặc khít 74%.
- Mạng tinh thể lập phương tâm khối có độ đặc khít 68%.
3. Liên kết kim loại
- Liên kết kim loại: là liên kết được hình thành giữa các nguyên tử và ion kim loại trong mạng tinh thêt do sự tham gia của êlectron tự do.
Bài tập & Lời giải
Câu 3.(Trang 82 SGK)
Liên kết kim loại là gì? So sánh với liên kết ion và liên kết cộng hoá trị?
Xem lời giải
Câu 4.(Trang 82 SGK)
Mạng tinh thể kim loại loại gồm có
A. nguyên tử, ion kim loại và các electron độc thân.
B. nguyên tử, ion kim loại và các electron tự do.
C. nguyên tử kim loại và các electron độc thân.
D. ion kim loại và các electron độc thân.
Xem lời giải
Câu 5.(Trang 82 SGK)
Cho cấu hình electron: 1s22s22p6.
Dãy nào sau đây gồm các nguyên tử và ion có cấu hình electron như trên?
A. K+, Cl, Ar.
B. Li+, Br, Ne.
C. Na+, Cl, Ar.
D. Na+, F-, Ne.
Xem lời giải
Câu 6.(Trang 82 SGK)
Cation R+ có cấu hình electron ở phân lớp ngoài cùng là 2p6. Nguyên tử R là
A. F
B. Na
C. K
D. Cl
Xem lời giải
Câu 7.(Trang 82 SGK)
Hoà tan 1,44 gam một kim loại hoá trị II trong 150 ml dung dịch H2SO4 0,5M . Để trung hoà axit dư trong dung dịch thu được, phải dùng hết 30 ml dung dịch NaOH 1M. Kim loại đó là:
A. Ba
B. Ca
C. Mg
D. Be
Xem lời giải
Câu 8.(Trang 82 SGK)
Hoà tan hoàn toàn 15,4 gam hỗn hợp Mg và Zn trong dung dịch HCl dư thấy có 0,6 gam khí H2 bay ra. Khối lượng muối tạo ra trong dung dịch là?
A. 36,7 gam
B. 35,7 gam
C. 63,7 gam
D. 53,7 gam.
Xem lời giải
Câu 9.(Trang 82 SGK)
Cho 12,8 gam kim loại A hoá trị II phản ứng hoàn toàn với khí Cl2 thu được muối B. Hoà tan B vào nước để được 400 ml dung dịch C. Nhúng thanh sắt nặng 11,2 gam vào dung dịch C, sau một thời gian thấy kim loại A bám vào thanh sắt và khối lượng thanh sắt lúc này là 12,0 gam; nồng độ FeCl2 trong dung dịch là 0,25M. Xác định kim loại A và nồng độ mol của muối B trong dung dịch C.